Molekylaid hápmi mearrida fysalaš iešvuođaid

Fámut mat doibmet molekylaid gaskkas leat mihá geahnoheappot go fámut mat doibmet atomaid gaskkas, ovdamearkka dihte kovaleanta čanastagat.
Lea dábálaš juohkit famuid molekylaid gaskkas golmma jovkui:
- fámut eahpepolára molekylaid gaskkas
- fámut polára molekylaid gaskkas
- hydrogenačanastagat
Elektrovnnat lihkadit čađa gaskka. Elektrovdnabárra mii juhkko dássedit guovttii hydrogenatoma gaskkas H-H ovttastusas, sáhttá dan dihte oanehaš botta leat lagabus ovtta H-atoma go dan nuppi.
Dalle čuožžila láddagaserohus, ja molekyla oažžu ovtta negatiiva pola ja ovtta positiiva pola. Nuppi čalbmeravkaleamis gessojuvvo elektrovdnabárra nuppe guvlui, ja molekyla láddagas šaddá nuppe gežiid. Nie joatká, ja goabbá pola lea positiiva ja goabbá lea negatiiva lotnahuvvá čađat. Diekkár molekylaid gohčodit mii gaskaboddosaš dipolan.
Dát gaskaboddosaš láddagaserohus dahká ahte eahpepolára molekylat maid sáhttet bissut čoahkis muhtin muddui. Dat geasuheaddji fámut mat čuožžilit leat gal geahnoheamit, ja ii dárbbaš ollu "gaikut" molekylaid eret nubbi nuppis.
Mađi stuorát mássa, dađi gievrrat fámut
Fámut gaskaboddosaš dipolaid gaskkas leat geahnoheamit, ja molekylain ii sáhte guhkes gaskka leat vai dát fámut vaikkuhit daidda. Fámut leat gievrrabut dađi stuorát mássa atomain lea.
Tabealla vuolábealde čajeha halogenaid sirrejuvvon mássa mielde:
Oktavuohta | mássa, u | ||
|---|---|---|---|
fluormolekyla | 38 | –220 | –188 |
kloramolekyla | 71 | –101 | 35 |
bromamolekyla | 160 | 7 | 59 |
jodamolekyla | 254 | 114 | 184 |
Fluoris lea vuollegis suddan- ja duldenčuokkis, nu ahte dárbbašuvvo unnán energiija sirret fluormolekylaid.
Jodas lea alla suddan- ja duldenčuokkis. Dárbbašuvvo dan dihte ollu energiija oažžut joda suddat dahje duldet, go leat oalle gievrras fámut mat doibmet jodamolekylaid gaskkas.
Dát doallá bures deaivasa dainna ahte fámut mat doibmet molekylaid gaskkas, leat gievrrabut atomaide main lea stuora mássa go atomaide main lea unna mássaš.
Mađi eambbo oktavuohta bajildusaid gaskkas, dađi gievrrat fámut

Leat go geahččalan rahpat stuora lohkkabátti? Dalle fertet geavahit oalle ollu fámuid! Lea mihá álkit rahpat lohkkabátti mas lea unnit bajildus. Das eai leat liika máŋga fakki mat darvanit nuppi oasi fakkiid duohkai.
Mii beassat oaidnit ahte seeammasullasaš prinsihppa gusto molekylaide.
Ávdnasat vuolábealde leat buohkat huksejuvvon 5 karbonatomas ja 12 hydrogenatomas. Dain lea nappo seamma mássa. Dain leat aŋke ieáguđetlágan duldenčuoggát.
Go ávnnas lea golgi hámis, de leat fámut molekylaid gaskkas mat dagahit ahte molekylat bissot oalle čoahkis. Jus mii lasihit temperatuvrra golgosis, de energiija mii lasihuvvo, lea doarvái stuoris gaikut molekylaid eret nubbi nuppis.
Jus muhtin ávdnasa duldenčuokkis lea vuollegaš, de dat muitala ahte fámut molekylaid gaskkas eai leat beare gievrrat. Neopentánas lea vuolimus duldenčuokkis dáin ávdnasiin. Dat mearkkaša ahte fámut mat dollet neopentánamolekylaid čoahkis, leat geahnoheappot go fámut mat dollet isopentánamolekylaid čoahkis.
Ávdnasiid bajildus čilge ášši. Neopentánas lea kuvlahápmi ja das lea dan dihte unnán oktavuohta eará neopentánamolekylaid bajildusaiguin. N-pentan lea eambbo guhkolaš. Dat addá eambbo oktavuođa eará n-pentánamolekylaid bajildusaiguin ja stuorát guovlluid gos čánastagat sáhttet ávdnejuvvot.
Fámut mat doibmet eahpepolára molekylaid gaskkas, lassanit go
- molekylaid mássa lassana
- molekylaid bajildusaid oktavuohta lassana
Polára molekylas lea ovtta oasis molekylas unna, positiiva láddágas, seammás go eará oasis lea unna, negatiiva láddagas. Mii dadjat ahte molekyla lea dipola. HCl lea ovdamearka molekylii mii lea (bistevaš) dipola.
Polára molekylat bissot čoahkis daid geasuheaddji fámuid geažil mat leat vuostelas láddagasaid gaskkas molekylain mat leat lahkalaga.
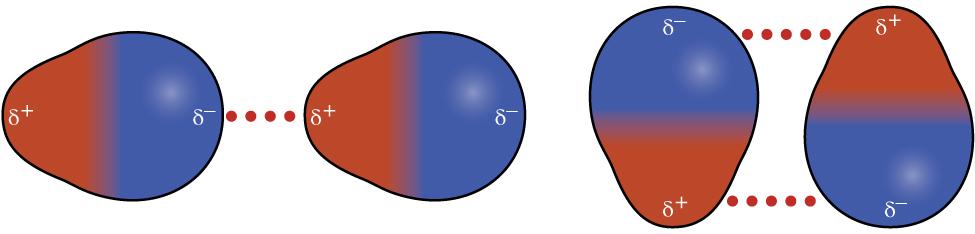
Dát fámut leat mihá gievrrabut go buohtastahttá fámguiguin mat leat gaskaboddosaš dipolaid gaskkas. Tabeallas vuolábealde oaidnit ahte fluora duldenčuokkis lea mihá vuollelis go sáltesuvrri duldenčuokkis. Lea nappo álkit duldehit fluora go sáltesuvrri.
Čilgehus lea čanastagain molekylaid gaskkas: Fluormolekylat leat gaskaboddosaš dipolat. Famut mat doibmet gaskaboddosaš dipolaid gaskkas, leat mihá geahnoheappot go fámut mat doibmet HCl bistevaš dipolaid gaskkas.
Iešvuohta | HCl | F2 |
|---|---|---|
molekylálossodat | 36,5 u | 38 u |
duldenčuokkis | –85 °C | –188 °C |
molekyla lea | bistevaš dipola | gaskaboddosaš dipola |