Ionebinding

Ionebinding – metall og ikke-metall
Ionebinding dannes når ioner med motsatt ladning tiltrekkes av hverandre. For eksempel: Når metallet natrium reagerer med ikke-metallet klor, gir natrium fra seg ett elektron og blir et positivt ion (Na⁺). Klor tar imot elektronet og blir et negativt ion (Cl⁻). Tiltrekningen mellom de positive og negative ionene er det som utgjør selve ionebindingen.

Ioneforbindelser er salter
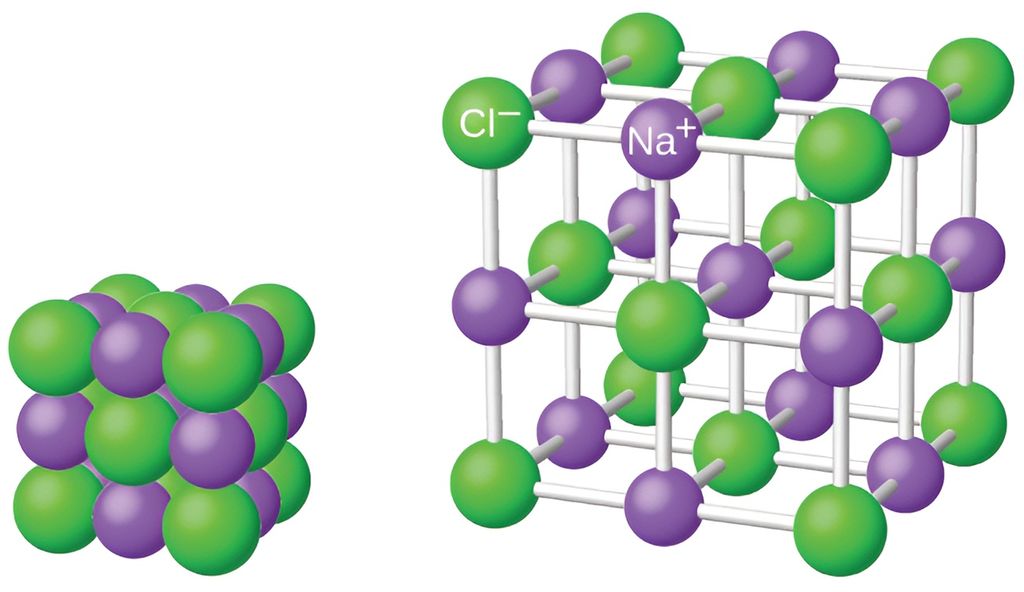
En ionebinding oppstår når positive og negative ioner tiltrekker hverandre, og ionene bygger opp store nettverk kalt ionegitre. Tiltrekningskreftene i disse gitrene er svært sterke, siden hvert ion binder seg til flere ioner i ulike retninger. Derfor regnes ionebinding som en av de sterkeste kjemiske bindingene.
Ioneforbindelser er stoffer der atomene holdes sammen av ionebindinger, og slike forbindelser omtales ofte som salter. Ordet "salt" brukes i naturfag i en videre betydning enn i dagligtale. Vanligvis mener vi bordsalt (NaCl) når vi sier "salt", men i naturfag brukes begrepet om alle forbindelser der ionebinding holder atomene sammen.
Egenskaper til salter
Fordi salter er bygd opp av sterke ionebindinger i et ionegitter, får de noen typiske egenskaper.
De er sprø
Ionegitteret er sterkt, men ikke fleksibelt. Hvis lagene skyves i forhold til hverandre, vil ioner med samme ladning havne ovenfor hverandre og frastøte hverandre. Derfor er salter sprø, og de sprekker lett.
De har høyt smeltepunkt og kokepunkt
Det kreves også mye energi for å bryte opp ionebindinger, noe som forklarer at salter har høyt smeltepunkt og kokepunkt.
De kan lede strøm
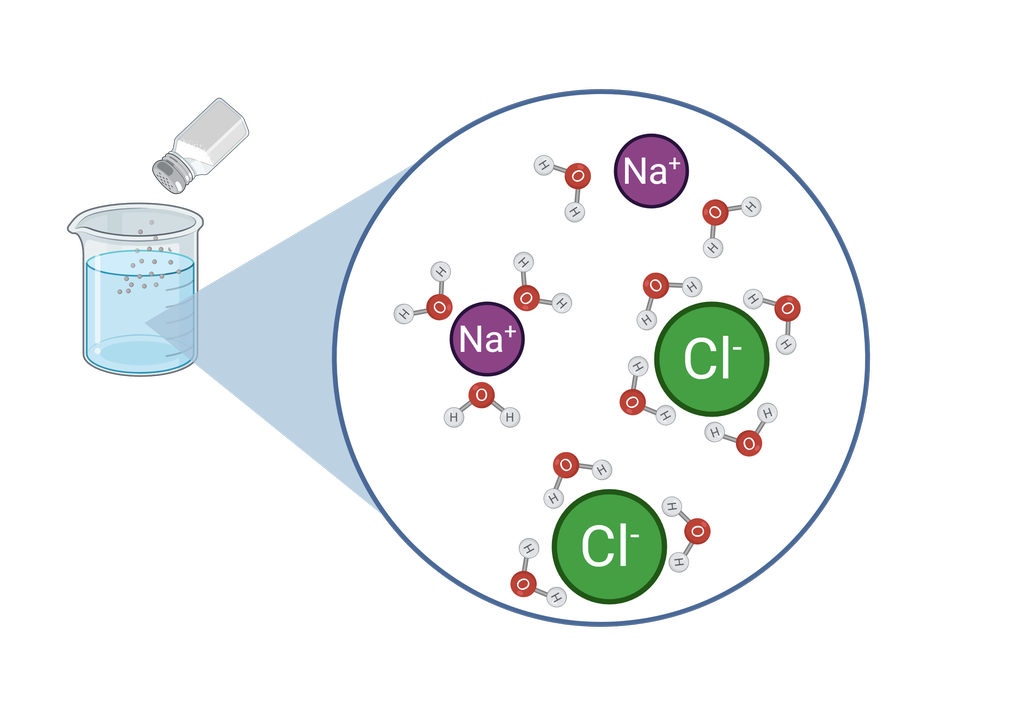
I fast form er ionene låst i ionegitteret, og de leder strøm dårlig. Men hvis saltet løses i vann, frigjøres ionene, og de kan lede strøm godt.
Oppgaver
Velg rett alternativ.