Organiske stoff

Organiske stoff – karbon er sentralt
Alle organiske sambindingar har karbon som ein del av strukturen sin. Det finst berre nokre sambindingar med karbon som blir rekna som uorganiske. Dei vanlegaste døma på uorganiske karbonsambindingar er karbondioksid og karbonsyre/kolsyre ()
Hydrokarbon – kjeder med karbon og hydrogen
Stoff som består av berre hydrogen og karbon, blir kalla hydrokarbon. Karbonatoma er bundne saman i kjeder av varierande lengd.
Alkan – karbonkjeder utan dobbeltbindingar
Alkan er karbonkjeder av varierande lengd utan dobbeltbindingar mellom karbonatoma. Fordi alle karbonatoma har bindingar til fire andre atom, er det på ein måte ikkje plass til fleire atom. Dette gjer at alkana ikkje reagerer lett med andre stoff.

Alken – karbonkjeder med dobbeltbinding

Alken er bygde opp av karbonkjeder med ei eller fleire dobbeltbindingar mellom karbonatoma. Molekyl med dobbeltbinding er umetta. Alken er dermed umetta hydrokarbon.
Dobbeltbindingane i alken gjer at desse stoffa reagerer lettare med andre stoff enn det alkan gjer. Når dobbeltbindingar blir brotne opp, blir det ledige elektron som kan danne bindingar til andre stoff.
Alken kan brukast som utgangspunkt for å lage plast. Plasten polyeten (PE) består av mange etenmolekyl som har reagert og danna lange kjeder.

Alkyn – karbonkjeder med trippelbinding
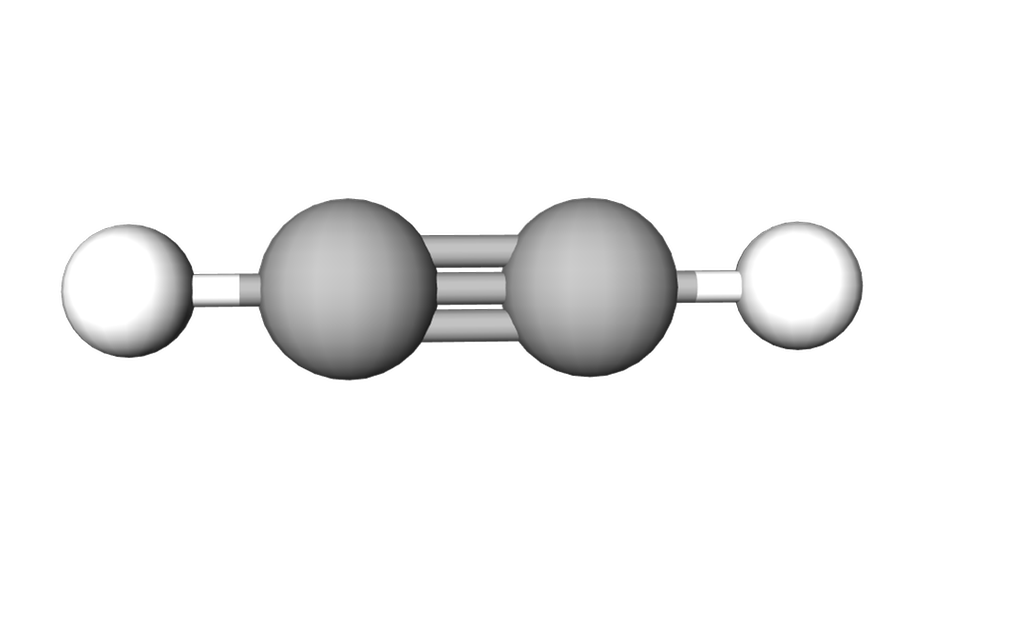
I gruppa alkyn finn vi stoff som består av karbonkjeder med ei eller fleire trippelbindingar.
Det enklaste alkynet består av to karbonatom og blir kalla etyn. Stoffet er meir kjent under namnet acetylen eller sveisegass.
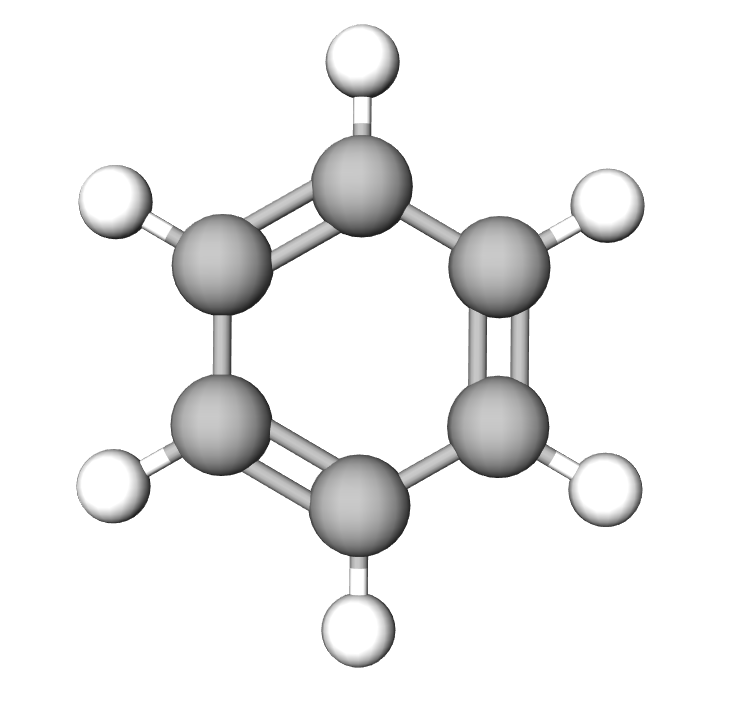
Aromatiske hydrokarbon – karbonkjeda utgjer ein ring
Hydrokarbon som dannar ringforma strukturar, blir kalla aromatiske hydrokarbon. Opphavleg gjaldt denne nemninga sambindingar som var avleidde frå eit stoff som heiter benzen. Benzen har ei søtleg lukt, og derfor blei sambindinga omtala som aromatisk. I dag blir nemninga brukt om alle hydrokarbon med ringforma strukturar. Benzen blir brukt i bensin. Viss du er blant dei som synest bensin luktar godt, er det benzen som er forklaringa på lukta. Sjølv om bensin har ein god aroma, er det ingen god idé å lukte for mykje på bensinen – benzen er kreftframkallande.
Alkoholar
I daglegtale bruker vi omgrepet alkohol når vi omtalar etanol eller sprit. Etanol er berre eitt av mange stoff som høyrer til gruppa alkoholar.
Eigenskapar
Dei enklaste alkoholane er flytande ved romtemperatur. Dei er polare og blir derfor lett løyste i vatn.
Kjemisk oppbygnad
Viss vi tek utgangspunkt i hydrokarbonet etan og byter ut eitt H-atom med ei hydroksylgruppe (), får vi alkoholen etanol. Legg merke til at denne hydroksylgruppa () ikkje er den same som hydroksidgruppa () vi kjenner frå basar.

Bruk og førekomst
Nokre typar gjærsopp dannar etanol når dei forbrenn sukker. Dette blir utnytta i produksjon av øl og vin.

Alkoholen glyserol er ein av byggjesteinane i feitt.
Organiske syrer
Viss du lèt ei flaske raudvin stå framme utan kork, vil det etter kvart oppstå ei sur lukt. Bakteriar dannar etanol i raudvinen om til eddiksyre (etansyre) ved hjelp av oksygen frå lufta.
Eddiksyre () og alle andre organiske syrer har ei karboksylgruppe (). Ein syre-base-reaksjon kan føre til at denne gruppa gir frå seg på same måte som i andre syrer.
Når kroppen dannar næringsstoff om til energi, og har lite tilgang på oksygen, blir mjølkesyre (laktat) danna som eit biprodukt. Mjølkesyre blir òg brukt som ingrediens i kosmetiske produkt og næringsmiddel.