Ionebinding

Ionebinding – metall og ikkje-metall
Ionebinding blir danna når ion med motsett ladning blir tiltrekte av kvarandre. Til dømes: Når metallet natrium reagerer med ikkje-metallet klor, gir natrium frå seg eitt elektron og blir eit positivt ion (Na⁺). Klor tek imot elektronet og blir eit negativt ion (Cl). Tiltrekkinga mellom dei positive og negative iona er det som utgjer sjølve ionebindinga.

Ionesambindingar er salt
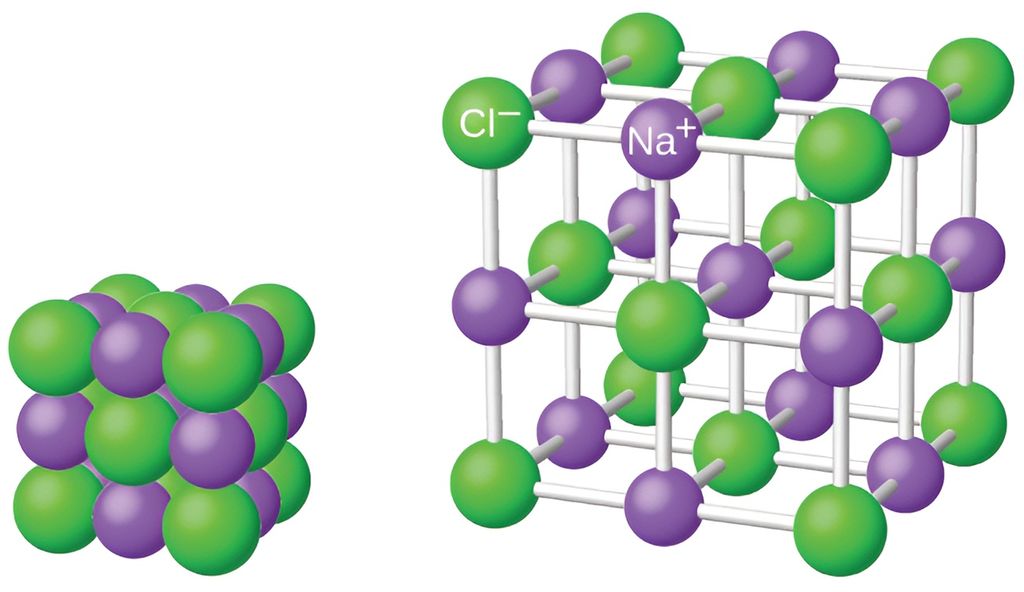
Ei ionebinding oppstår når positive og negative ion tiltrekker kvarandre, og iona bygger opp store nettverk kalla ionegitter. Tiltrekkingskreftene i desse gittera er svært sterke, sidan kvart ion bind seg til fleire ion i ulike retningar. Derfor blir ionebinding rekna som ei av dei sterkaste kjemiske bindingane.
Ionesambindingar er stoff der atoma blir haldne saman av ionebindingar, og slike sambindingar blir ofte kalla salt. Ordet "salt" blir brukt i naturfag i ei vidare betydning enn i daglegtale. Vanlegvis meiner vi bordsalt (NaCl) når vi seier "salt", men i naturfag blir omgrepet brukt om alle sambindingar der ionebinding held atoma saman.
Eigenskapar til salt
Fordi salt er bygde opp av sterke ionebindingar i eit ionegitter, får dei nokre typiske eigenskapar.
Dei er sprø
Ionegitteret er sterkt, men ikkje fleksibelt. Viss laga blir skyvde i forhold til kvarandre, vil ion med same ladning hamne ovanfor kvarandre og fråstøyte kvarandre. Derfor er salt sprø, og dei sprekk lett.
Dei har høgt smeltepunkt og kokepunkt
Det krevst òg mykje energi for å bryte opp ionebindingar, noko som forklarer at salt har høgt smeltepunkt og kokepunkt.
Dei kan leie straum
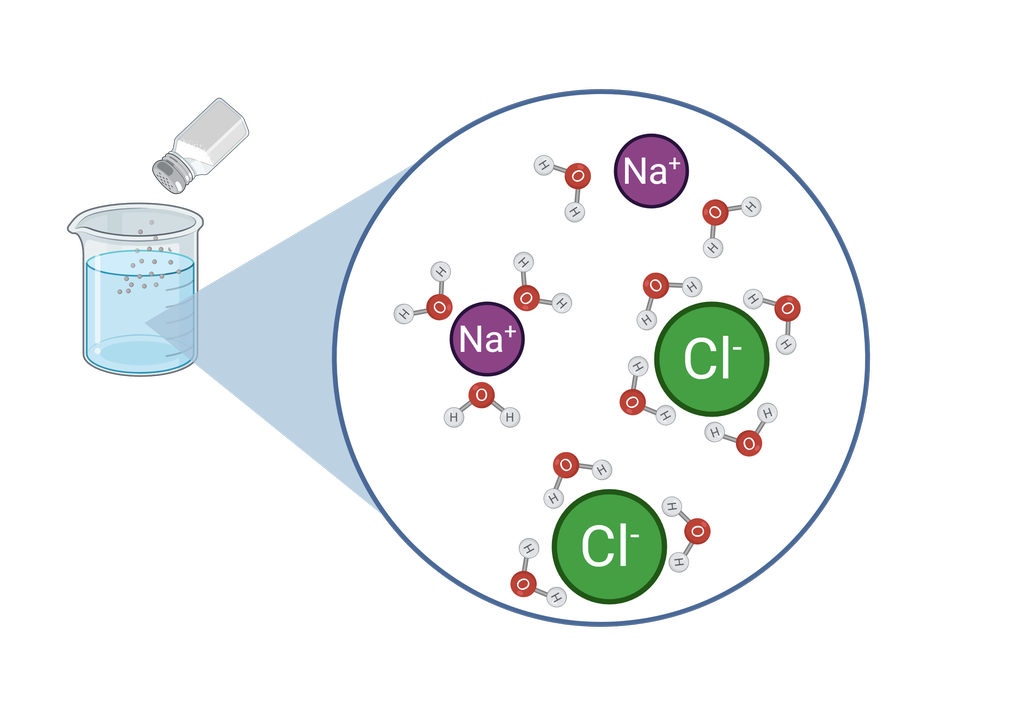
I fast form er iona låste i ionegitteret, og dei leier straum dårleg. Men viss saltet blir løyst i vatn, blir iona frigjorde, og dei kan leie straum godt.
Oppgåver
Vel rett alternativ.