Fagartikkel
Batterier
Batterier er en genial måte å lagre energi på. Her er det kjemisk energi som kan omformes til elektrisk energi når man trenger strøm. Siden det første galvaniske element, har batteriene blitt svært mye mindre og mer effektive, hva tenker du om det miljømessige?
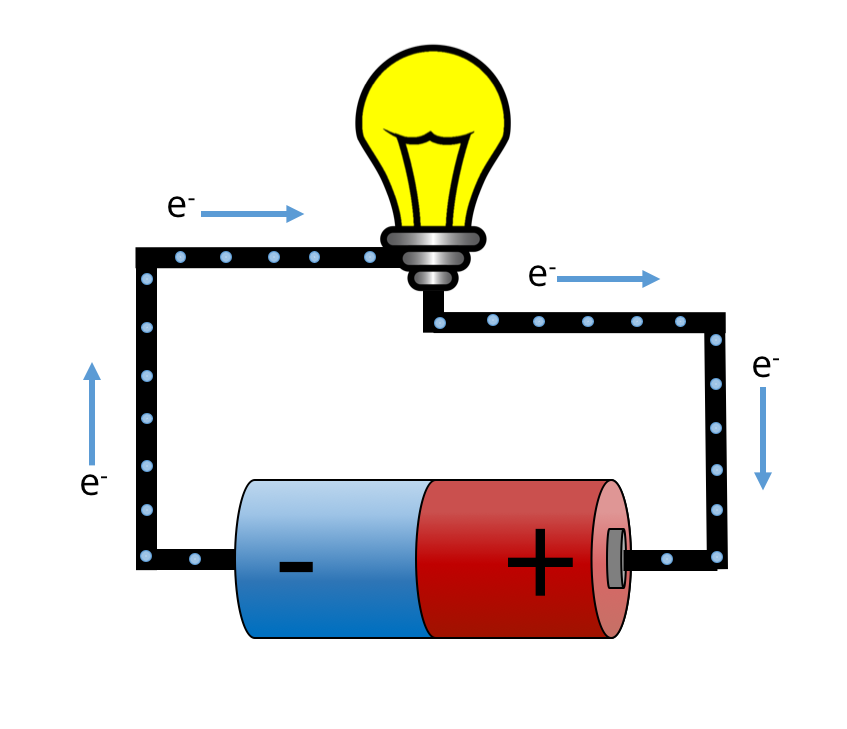
Elektronene beveger seg fra den negative polen (–) til den positive polen (+) på batteriet. Strømretningen er definert til å være det motsatte av dette. Bilde: UngEnergi / CC BY-NC-SA 4.0
- 1800 – Den italienske vitenskapsmannen Alessandro Volta fant opp det første kjemiske batteriet.
- 1859 – Det første oppladbare blybatteriet ble laget av den franske fysikeren Gaston Planté.
- 1890 – Porsche bygde sine første biler. Disse var faktisk elektriske! Porsche brukte blybatterier i bilene sine.
- 1899 – Svenske Waldemar Jungner finner opp Nikkel-kadmium-batteriet (NiCd). Dette batteriet er også oppladbart, men det har en høyere energitetthet og er mer robust enn blybatteriet.
- 1980 – Først nå kommer de moderne batteritypene. Vi får etter hvert nikkel-hydrogenbatterier (NiMH -nikkel-metallhydrid) og litiumbatterier (Li).
Relatert innhold
For å lage en galvanisk celle trenger vi to forskjellige metaller og en elektrolytt. Spenningen mellom to metallelektroder er avhengig av hvor metallene er plassert i spenningsrekken.
Jo større avstand det er mellom dem i spenningsrekken, desto større blir spenningen.
Et batteri består av flere galvaniske celler/elementer.
Bruk spenningsrekka under til å forutsi hva som skjer hvis for eksempel jern-metall (Fe) og kobber-ioner () kommer i kontakt med hverandre.
Velg ett metall i kolonnen til venstre og klikk på ett metall-ion i kolonnen til høyre for å se om det kan overføres elektroner.
Trodde du rett?