Organiske stoffer

Alle organiske forbindelser har karbon som en del av strukturen sin. Det finnes bare noen forbindelser med karbon som regnes som uorganiske. De vanligste eksemplene på uorganiske karbonforbindelser er karbondioksid og karbonsyre/kullsyre (
Stoffer som består av bare hydrogen og karbon, kalles hydrokarboner. Karbonatomene er bundet sammen i kjeder av varierende lengde.
Alkaner – karbonkjeder uten dobbeltbindinger
Alkaner er karbonkjeder av varierende lengde uten dobbeltbindinger mellom karbonatomene. Fordi alle karbonatomene har bindinger til fire andre atomer, er det på en måte ikke plass til flere atomer. Dette gjør at alkanene ikke reagerer lett med andre stoffer.
Alkener – karbonkjeder med dobbeltbinding
Alkener er bygd opp av karbonkjeder med én eller flere dobbeltbindinger mellom karbonatomene. Molekyler med dobbeltbinding er umettede. Alkener er dermed umettede hydrokarboner.
Dobbeltbindingene i alkener gjør at disse stoffene reagerer lettere med andre stoffer enn det alkaner gjør. Når dobbeltbindinger brytes opp, blir det ledige elektroner som kan danne bindinger til andre stoffer.
Alkener kan brukes som utgangspunkt for å lage plast. Plasten polyeten (PE) består av mange etenmolekyler som har reagert og dannet lange kjeder.
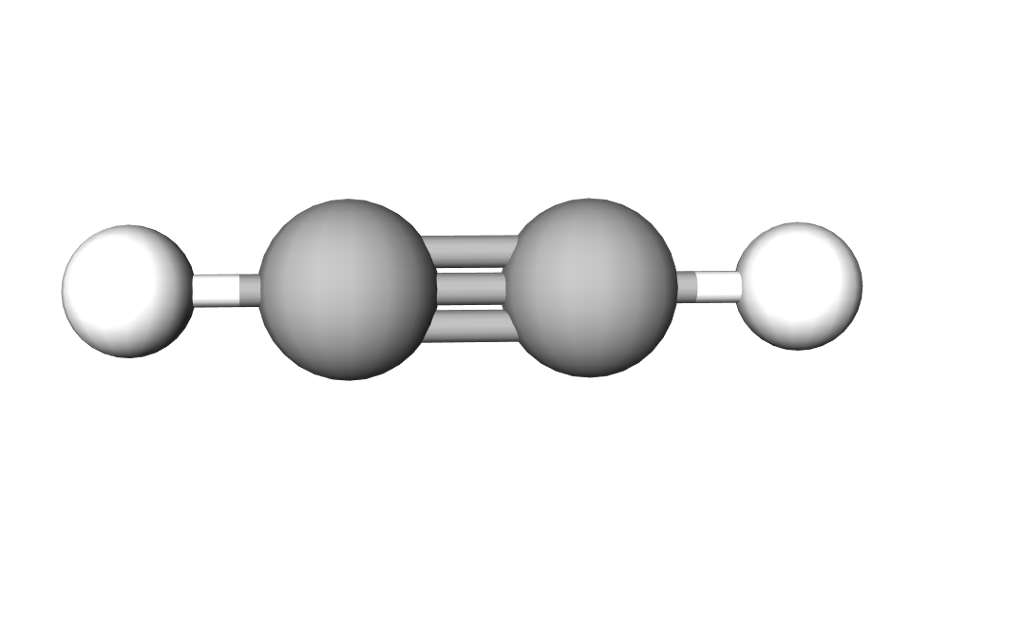
Alkyner – karbonkjeder med trippelbinding
I gruppa alkyner finner vi stoffer som består av karbonkjeder med én eller flere trippelbindinger.
Det enkleste alkynet består av to karbonatomer og kalles etyn. Stoffet er mer kjent under navnet acetylen eller sveisegass.
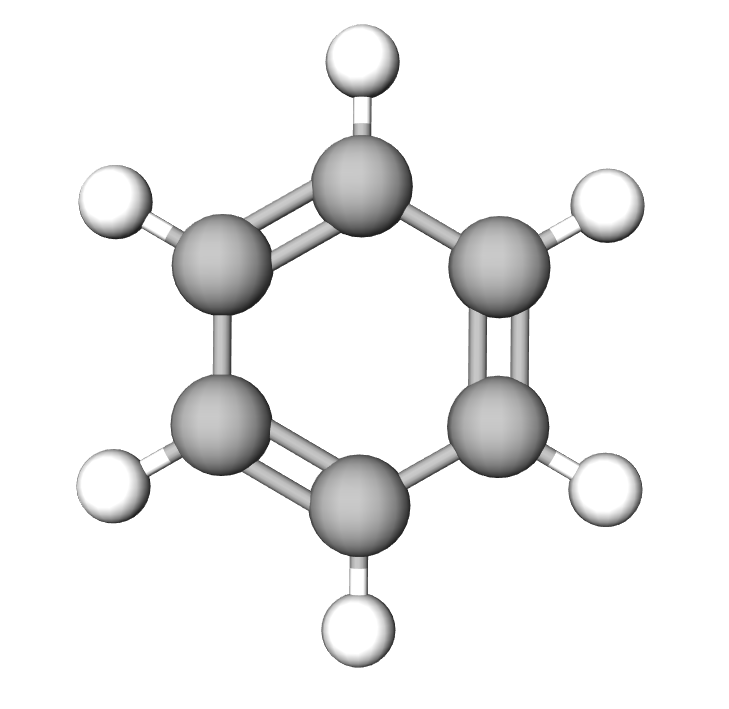
Aromatiske hydrokarboner – karbonkjeden utgjør en ring
Hydrokarboner som danner ringformede strukturer, kalles aromatiske hydrokarboner. Opprinnelig gjaldt denne betegnelsen forbindelser som var avledet fra et stoff som heter benzen. Benzen har ei søtlig lukt, og derfor ble forbindelsen omtalt som aromatisk. I dag brukes betegnelsen om alle hydrokarboner med ringformede strukturer. Benzen brukes i bensin. Hvis du er blant dem som synes bensin lukter godt, er det benzen som er forklaringen på lukta. Selv om bensin har en god aroma, er det ingen god idé å lukte for mye på bensinen – benzen er kreftframkallende.
I dagligtale bruker vi begrepet alkohol når vi omtaler etanol eller sprit. Etanol er bare ett av mange stoffer som tilhører gruppa alkoholer.
Egenskaper
De enkleste alkoholene er flytende ved romtemperatur. De er polare og løses derfor lett i vann.
Kjemisk oppbygning
Hvis vi tar utgangspunkt i hydrokarbonet etan og bytter ut ett H-atom med ei hydroksylgruppe (
Bruk og forekomst
Noen typer gjærsopp danner etanol når de forbrenner sukker. Dette utnyttes i produksjon av øl og vin.
Alkoholen glyserol er en av byggesteinene i fett.
Hvis du lar ei flaske rødvin stå framme uten kork, vil det etter hvert oppstå ei sur lukt. Bakterier omdanner etanol i rødvinen til eddiksyre (etansyre) ved hjelp av oksygen fra lufta.
Eddiksyre (
Når kroppen omdanner næringsstoffer til energi, og har lite tilgang på oksygen, dannes melkesyre (laktat) som et biprodukt. Melkesyre brukes også som ingrediens i kosmetiske produkter og næringsmidler.